DÉCOUVREZ LES PRINCIPES THÉORIQUES ESSENTIELS
DE L’ÉLECTROPHORÈSE CAPILLAIRE
L’Electrophorèse Capillaire (EC) est une technique de séparation analytique.
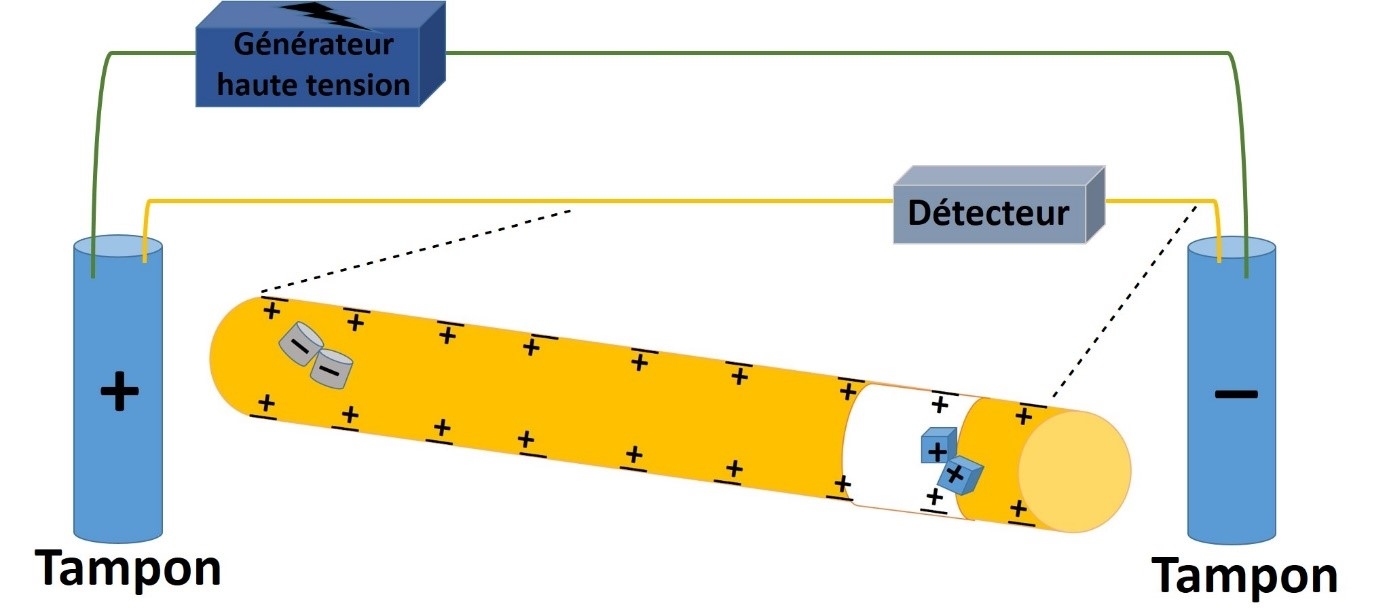
Les composés du mélange sont injectés dans un capillaire, le plus fréquemment de silice vierge et sont séparés à l’aide d’un tampon sous l’effet d’un champ électrique grâce à leurs différences de mobilités. Un détecteur permet ensuite de visualiser cette séparation sur un électrophérogramme.
L’EC PERMET D’INJECTER DE FAIBLES VOLUMES
L’Electrophorèse Capillaire permet de n’injecter que quelques nanolitres d’échantillon. Il existe deux modes d’injection différents :
- L’injection hydrodynamique : application d’une surpression à l’entrée du capillaire (ou le vide à la sortie du capillaire) pour introduire l’échantillon à l’intérieur
- L’injection électrocinétique : application d’une tension aux bornes du capillaire. Cette tension permet aux composés ionisés ou entraînés par électroosmose de pénétrer à l’intérieur du capillaire
LE TRANSPORT DES COMPOSÉS
Le transport des composés à l’intérieur du capillaire est régi par deux phénomènes : l’écoulement électroosmotique (électroosmose) et la migration électrophorétique.
L’électroosmose
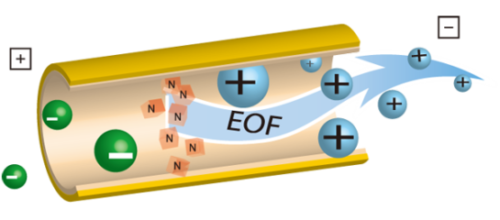
La paroi du capillaire est recouverte de groupements silanol qui se déprotonent si le pH est supérieur à 2,5. Les groupements silanol déprotonés forment une couche de charges négatives à la surface du capillaire. Les cations solvatés présents dans l’électrolyte viennent alors se positionner en regard pour former une double couche électrique. Ces cations se mettent en mouvement dès qu’un champ électrique est créé dans le capillaire, entraînant les autres molécules. L’écoulement qui en résulte possède un profil de vitesse plat et est dirigé de l’anode vers la cathode. Cet écoulement électroosmotique peut être modifié : inversé, annulé avec un capillaire greffé ou en adsorbant sur la paroi du capillaire des tensioactifs ou des polymères neutres ou chargés.
La migration électrophorétique
La séparation des composants par Electrophorèse Capillaire dépend de leur différence de vitesse de migration. La mobilité électrophorétique d’un ion tient compte des conditions opératoires tels que le pH, la force ionique, la composition et la viscosité de l’électrolyte de séparation.
L’EC est reconnue aujourd’hui pour ses séparations rapides, efficaces et hautement résolutives, sa faible consommation de solvant et son coût de fonctionnement minime. Elle apparait comme une technique de choix pour permettre de relever les défis analytiques auxquels la chromatographie en phase liquide ne peut pas répondre ou bien apporter un complément ou une confirmation des résultats déjà obtenus.
Les modes des séparations
Tout comme la chromatographie en phase liquide, l’EC a développé de nombreux modes de séparation.
L’Electrophorèse Capillaire de zone (CZE) va permettre l’analyse de composés ionisés ou ionisables (à caractères acido-basiques). Les analytes sont alors séparés selon leur rapport charge / rayon hydrodynamique et migrent vers le pôle de signe opposé. Les composés neutres ne sont pas séparés avec ce mode d’analyse. L’électrophorèse de zone est le mode de mise en œuvre le plus simple de l’Electrophorèse Capillaire.
La Chromatographie Electrocinétique micellaire (MEKC) est destinée aux composés neutres ou aux composés chargés difficilement séparables. On ajoute alors à l’électrolyte un tensioactif pour qu’il se forme des micelles dont la partie intérieure est hydrophobe. Ces micelles créent une pseudo-phase stationnaire dans le capillaire et la séparation se fait alors selon un mécanisme de partage.
La CE est aussi reconnue pour être performante dans l’analyse de composés chiraux. Avec l’ajout de sélecteurs chiraux dans l’électrolyte (Cyclodextrines par exemples), il est possible de séparer des énantiomères.
L’Electrophorèse Capillaire sur gel (CGE) permet de séparer des molécules en fonction de leur taille. Très utilisé notamment pour l’analyse de protéines, ce mode de séparation est mis en œuvre à l’aide d’un capillaire rempli d’un électrolyte contenant un gel qui stabilise le milieu contre le phénomène de convection et joue le rôle de tamis moléculaire.
La CE peut être enfin utilisée avec un capillaire rempli :
- D’une phase stationnaire de chromatographie (on parle alors d’électrochromatographie capillaire)
- D’un mélange ampholytes créant un gradient de pH croissant de l’anode à la cathode (focalisation isoélectrique, IEF)
- De plusieurs tampons de conductivités variables (isotachophorèse capillaire, ITP).
LA DÉTECTION DES COMPOSÉS
La détection UV est fournie commercialement sur tous les appareillages d’Electrophorèse Capillaire. Elle est réalisée directement à travers le capillaire au niveau d’une fenêtre réalisée en éliminant la couche de polyimide externe. La plupart des anions et cations inorganiques n’absorbant pas ou peu dans la zone UV-Visible. Ils ne peuvent donc pas être directement détectés. Pour pallier cette absence d’absorbance, de nombreuses méthodes impliquant une détection en UV indirecte ont été mises en œuvre avec l’utilisation d’agents visualisants ou chromophores.

D’autres types de détection sont possibles pour les espèces inorganiques, telle que la conductimétrie qui est une alternative intéressante. Cette technique de détection a pour avantage d’être universelle pour l’analyse d’espèces ioniques. Elle implique une mesure de conductance entre deux électrodes, qui peut être réalisée soit par contact entre l’électrolyte de séparation et les électrodes de mesure ou bien en mode sans contact dans lequel les électrodes se situent de part et d’autre du capillaire.
Enfin, pour les molécules organiques, des modes de détection tels que l’ampérométrie, la fluorimétrie ou bien la spectrométrie de masse ont été rapportés.
Les couplages CE / MS se sont énormément développés depuis la fin des années 80. Ce couplage présente cependant quelques difficultés de mise en œuvre, dont le maintien du contact électrique aux bornes du capillaire et l’obtention d’une bonne efficacité d’ionisation / désorption des analytes dans la source d’ionisation. Deux interfaces sont aujourd’hui fréquentes : les interfaces avec ou sans liquide additionnel. Les processus d’ionisation par électronébulisation, ionisation chimique à pression atmosphérique, ionisation photochimique à pression atmosphérique, ionisation par plasma à couplage inductif ICP / MS, ou par laser assistée par matrice (MALDI) sont aujourd’hui les modes d’ionisation les plus courants en CE.
Wynsep a mis au point une nouvelle génération d’Electrophorèse Capillaire
Découvrez l’Electrophorèse Capillaire Adaptative